Chào mừng bạn đến với Thế giới tai nghe, nơi chúng tôi không chỉ khám phá những công nghệ âm thanh tiên tiến mà còn mở rộng kiến thức sang các lĩnh vực đòi hỏi sự tập trung và độ chính xác cao, như kỹ thuật ngắm bắn. Trong nhiều hoạt động, từ thể thao đến quân sự, việc nắm vững nguyên tắc về đường ngắm là yếu tố quyết định sự thành công. Ngắm bắn không chỉ là một kỹ năng, mà còn là một nghệ thuật đòi hỏi sự phối hợp nhịp nhàng giữa mắt, tay và tinh thần. Việc hiểu rõ các khái niệm như đường ngắm cơ bản, điểm ngắm đúng và đường ngắm đúng sẽ giúp bạn cải thiện đáng kể khả năng của mình, không chỉ trong việc bắn súng mà còn trong bất kỳ hoạt động nào cần đến sự chính xác tuyệt đối.
Ngắm Bắn Là Gì? Vì Sao Nó Quan Trọng?
Ngắm bắn, về cơ bản, là quá trình xác định góc bắn và hướng bắn sao cho quỹ đạo của đường đạn đi qua điểm mà người bắn muốn chạm tới trên mục tiêu. Đây là một động tác tối quan trọng, quyết định trực tiếp đến việc viên đạn có trúng đích hay không. Để thực hiện một phát bắn chính xác, người bắn cần phải phối hợp một cách nhuần nhuyễn giữa việc định vị súng, điều chỉnh tầm ngắm và giữ cho mặt súng ở trạng thái thăng bằng. Nếu thiếu đi một trong những yếu tố này, kết quả bắn sẽ không đạt được như mong muốn, thậm chí có thể lệch mục tiêu hoàn toàn.
Trong mọi bài tập bắn súng, từ những buổi huấn luyện quân sự nghiêm ngặt cho đến các cuộc thi thể thao, kỹ thuật ngắm bắn luôn được đặt lên hàng đầu. Một xạ thủ giỏi không chỉ là người có phản xạ nhanh nhạy, mà còn phải là người hiểu sâu sắc về khoa học đằng sau mỗi phát bắn, đặc biệt là các nguyên lý liên quan đến đường ngắm. Đó là lý do vì sao chúng ta cần đi sâu vào từng khái niệm cốt lõi.
Đường Ngắm Cơ Bản: Nền Tảng Của Mọi Phát Bắn
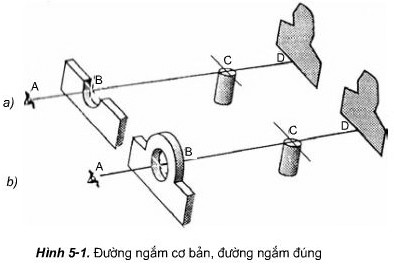
Đường ngắm cơ bản được định nghĩa là một đường thẳng tưởng tượng kéo dài từ mắt của người ngắm, đi qua chính giữa mép trên của khe ngắm và kết thúc tại điểm chính giữa mép trên của đầu ngắm. Đây là yếu tố nền tảng, là điểm xuất phát cho mọi thao tác ngắm bắn. Sự chính xác của đường ngắm cơ bản có ý nghĩa quyết định đến độ chính xác của góc bắn, cả về tầm xa lẫn hướng so với mục tiêu. Nếu đường ngắm cơ bản bị sai lệch ngay từ đầu, dù chỉ một chút, thì toàn bộ quá trình ngắm bắn phía sau sẽ trở nên vô nghĩa.
Hãy hình dung, khe ngắm và đầu ngắm trên súng hoạt động như hai điểm tham chiếu mà mắt chúng ta phải căn chỉnh thẳng hàng. Mắt người ngắm, khe ngắm và đầu ngắm cần nằm trên cùng một đường thẳng để tạo ra một đường ngắm cơ bản chuẩn xác. Đây là bước đầu tiên và cơ bản nhất mà mọi xạ thủ đều phải thành thạo. Việc luyện tập để đạt được đường ngắm cơ bản đúng đắn đòi hỏi sự kiên nhẫn và kỹ thuật nhất định, thường thông qua các bài tập lặp đi lặp lại để tạo thành phản xạ tự nhiên.
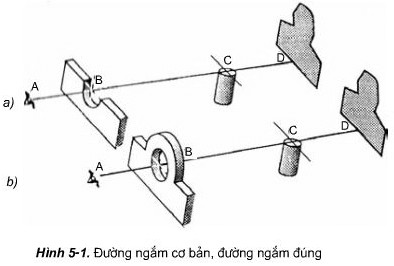 Mô tả đường ngắm cơ bản trong kỹ thuật bắn súng
Mô tả đường ngắm cơ bản trong kỹ thuật bắn súng
Điểm Ngắm Đúng: Xác Định Mục Tiêu Chính Xác
Điểm ngắm đúng là một khái niệm cực kỳ quan trọng, đó là điểm mà người bắn đã xác định từ trước trên mục tiêu. Khi ngắm vào điểm này và thực hiện phát bắn, quỹ đạo của đường đạn sẽ đi qua chính xác điểm định bắn trúng trên mục tiêu. Khác với đường ngắm cơ bản chỉ tập trung vào việc căn chỉnh các bộ phận của súng, điểm ngắm đúng liên quan trực tiếp đến vị trí cụ thể trên mục tiêu mà người bắn muốn tác động.
Việc chọn điểm ngắm đúng thường phụ thuộc vào nhiều yếu tố như cự ly bắn, loại súng, loại đạn, điều kiện thời tiết (gió, nhiệt độ) và thậm chí cả loại mục tiêu. Đôi khi, điểm ngắm đúng không phải là trung tâm của mục tiêu mà có thể là một vị trí dịch chuyển để bù trừ cho các yếu tố bên ngoài. Ví dụ, khi bắn vào các mục tiêu thấp ở cự ly xa, xạ thủ có thể cần chọn thước ngắm lớn hơn cự ly thực tế và ngắm vào mép dưới của mục tiêu để đảm bảo độ chính xác. Sự tinh tế trong việc lựa chọn điểm ngắm đúng đòi hỏi kinh nghiệm và khả năng phân tích tình huống của xạ thủ.
Đường Ngắm Đúng: Sự Kết Hợp Hoàn Hảo
Đường ngắm đúng là đỉnh cao của sự căn chỉnh, là sự kết hợp giữa đường ngắm cơ bản đã chính xác và việc dóng nó vào điểm ngắm đúng đã xác định trên mục tiêu, với một điều kiện tiên quyết là mặt súng phải thăng bằng. Nói cách khác, đường ngắm đúng là khi ba yếu tố – mắt người ngắm, bộ phận ngắm của súng và điểm ngắm trên mục tiêu – cùng nằm trên một đường thẳng hoàn hảo.
Để đạt được đường ngắm đúng, người bắn không chỉ cần có đường ngắm cơ bản chuẩn xác mà còn phải đảm bảo mặt súng không bị nghiêng lệch. Mặt súng thăng bằng có nghĩa là súng được giữ thẳng, không bị xoay về bên trái hay bên phải. Đây là một yếu tố thường bị bỏ qua nhưng lại có ảnh hưởng rất lớn đến kết quả bắn. Khi mặt súng thăng bằng, viên đạn sẽ bay theo quỹ đạo dự kiến. Nếu mặt súng bị nghiêng, viên đạn sẽ bị kéo thấp xuống và lệch về phía súng nghiêng, làm mất đi sự chính xác của phát bắn. Việc thực hành ngắm bắn liên tục và có sự điều chỉnh theo từng tình huống là chìa khóa để đạt được đường ngắm đúng một cách nhất quán.
Ảnh Hưởng Của Ngắm Sai Đến Kết Quả Bắn: Những Sai Lệch Thường Gặp
Trong kỹ thuật ngắm bắn, một sai lệch nhỏ cũng có thể dẫn đến kết quả hoàn toàn khác biệt. Có ba loại sai lệch chính khi ngắm bắn mà người học cần đặc biệt lưu ý:
1. Đường Ngắm Cơ Bản Sai Lệch
Nếu đường ngắm cơ bản không được căn chỉnh chính xác, điểm chạm của viên đạn trên mục tiêu sẽ bị ảnh hưởng nghiêm trọng. Cụ thể:
- Đầu ngắm thấp (hoặc cao) hơn khe ngắm: Nếu điểm chính giữa mép trên của đầu ngắm thấp hơn so với điểm chính giữa mép trên của khe ngắm, điểm chạm trên mục tiêu sẽ thấp hơn so với điểm định bắn trúng. Ngược lại, nếu đầu ngắm cao hơn, điểm chạm cũng sẽ cao hơn.
- Đầu ngắm lệch trái (hoặc phải) so với khe ngắm: Tương tự, nếu đầu ngắm lệch sang trái hoặc phải so với khe ngắm, điểm chạm trên mục tiêu cũng sẽ lệch về cùng phía so với điểm định bắn trúng.
Những sai lệch này cho thấy tầm quan trọng của việc căn chỉnh đường ngắm cơ bản một cách tỉ mỉ. Ngay cả một sai số nhỏ ở bộ phận ngắm cũng có thể khuếch đại thành một khoảng cách lớn trên mục tiêu, đặc biệt là ở cự ly xa.
2. Điểm Ngắm Sai
Khi đường ngắm cơ bản đã chính xác và mặt súng thăng bằng, nhưng điểm ngắm lại bị lệch so với điểm ngắm đúng, thì điểm chạm trên mục tiêu cũng sẽ sai lệch một khoảng tương ứng. Điều này có nghĩa là, nếu bạn ngắm sai một centimet so với điểm đích, viên đạn cũng sẽ chạm vào một điểm cách đích một centimet.
Ví dụ, nếu mục tiêu là một vòng tròn và điểm ngắm đúng là trung tâm, nhưng bạn lại ngắm vào mép trên của vòng tròn, thì viên đạn sẽ chạm vào một điểm cao hơn so với trung tâm. Sai lầm này thường xuất phát từ sự thiếu tập trung, đánh giá sai cự ly hoặc không điều chỉnh thước ngắm phù hợp với điều kiện thực tế. Đây là lý do vì sao việc huấn luyện về nhận diện mục tiêu và xác định điểm ngắm là rất cần thiết.
3. Mặt Súng Không Thăng Bằng
Đây là một trong những lỗi phổ biến nhưng thường bị bỏ qua bởi những người mới bắt đầu. Ngay cả khi đường ngắm cơ bản và điểm ngắm đã được xác định đúng, nếu mặt súng bị nghiêng về một phía, điểm chạm trên mục tiêu sẽ không chỉ thấp hơn mà còn lệch về phía súng bị nghiêng.
Hiện tượng này xảy ra do trọng lực và các yếu tố khí động học tác động lên viên đạn. Khi súng nghiêng, nòng súng không còn song song với mặt đất theo chiều ngang, làm cho quỹ đạo bay của đạn thay đổi. Đây là một lỗi kỹ thuật cần được khắc phục thông qua việc luyện tập tư thế giữ súng chắc chắn, cân bằng và duy trì trạng thái ổn định trong suốt quá trình ngắm và bóp cò.
Nâng Cao Kỹ Thuật Ngắm Bắn: Hơn Cả Lý Thuyết
Việc nắm vững lý thuyết về đường ngắm là bước khởi đầu, nhưng để trở thành một xạ thủ giỏi, việc luyện tập và thực hành là không thể thiếu. Một số lời khuyên để nâng cao kỹ năng ngắm bắn bao gồm:
- Luyện tập thường xuyên: Giống như bất kỳ kỹ năng nào khác, sự lặp lại tạo nên sự thành thạo. Việc thường xuyên tập trung vào việc lấy đường ngắm cơ bản, xác định điểm ngắm và giữ mặt súng thăng bằng sẽ giúp hình thành phản xạ tự nhiên.
- Kiểm soát hơi thở: Hơi thở ảnh hưởng rất lớn đến độ ổn định của cơ thể. Học cách kiểm soát hơi thở, giữ nhịp thở đều và thực hiện động tác bóp cò giữa hai nhịp thở sẽ giúp giảm thiểu rung động và tăng độ chính xác.
- Bóp cò êm, đều: Động tác bóp cò cần được thực hiện một cách nhẹ nhàng, đều đặn và thẳng trục nòng súng về phía sau cho đến khi đạn nổ, tránh giật cò hoặc bóp mạnh gây lệch súng. Sự giật cục khi bóp cò là một trong những nguyên nhân hàng đầu khiến đạn đi lệch.
- Phân tích kết quả bắn: Sau mỗi loạt bắn, việc phân tích điểm chạm trên mục tiêu là rất quan trọng để hiểu được những sai sót và điều chỉnh kỹ thuật cho những lần sau. Điều này giúp xạ thủ rút ra kinh nghiệm và cải thiện hiệu suất.
Những yếu tố này không chỉ áp dụng trong lĩnh vực quân sự hay thể thao bắn súng, mà còn có thể được liên hệ với nhiều khía cạnh khác của cuộc sống, nơi sự chính xác và tập trung là chìa khóa thành công.
Kết Luận
Hiểu rõ về đường ngắm là một trong những bài học đầu tiên và quan trọng nhất đối với bất kỳ ai quan tâm đến kỹ thuật bắn súng. Từ khái niệm cơ bản về đường ngắm cơ bản, đến việc xác định điểm ngắm đúng và cuối cùng là đạt được đường ngắm đúng hoàn hảo, mỗi bước đều đòi hỏi sự chú tâm và luyện tập không ngừng. Những sai lệch dù nhỏ trong quá trình ngắm bắn cũng có thể tạo ra sự khác biệt lớn trên mục tiêu, khẳng định tầm quan trọng của việc nắm vững và thực hành kỹ thuật một cách chính xác.
Tại Thế giới tai nghe, chúng tôi tin rằng việc truyền tải những kiến thức chuyên sâu và đáng tin cậy là sứ mệnh của mình. Hy vọng rằng bài viết này đã cung cấp cho bạn cái nhìn toàn diện và sâu sắc về các yếu tố cấu thành nên một phát bắn chính xác. Việc rèn luyện sự tập trung và độ chính xác trong bất kỳ lĩnh vực nào cũng đều cần đến sự kiên trì và kiến thức đúng đắn.